Summary
SummaryGerm-cell of the testis is a highly treatable and curable condition. Several post-orchidectomy treatment strategies can be applied. From the medical oncologist perspective, most patients can be successfully treated with chemotherapy with survival rates similar to other treatment options. Acute and long-term consequences such as nausea, vomiting, nephro and ototoxicity due to cisplatin; secondary malignancies due to etoposide and Raynaud’s phenomenon and pulmonary toxicity caused by bleomycin; as well as a significant increase y cardiovascular mortality several years after both chemo and radiation therapy have to be considered when designing a treatment plan. For most patients, though, treatment is safe and effective and countless lives have been saved by it. A brief review of the stage by stage treatment recommendations is the focus of this article.
IntroducciónEl cáncer de testículo es el ejemplo más dramático de la eficacia de la quimioterapia antineoplásica en enfermedad avanzada. Antes del advenimiento de la quimioterapia basada en cisplatino, la inmensa mayoría de los pacientes con enfermedad metastásica sucumbían. En este documento pretendo resumir los conceptos globales de manejo inicial con quimioterapia en pacientes con tumores germinales del testículo. Para poder ubicar al lector, se requiere de una breve descripción del sistema de estadificación, el concepto de riesgo para enfermedad avanzada y aspectos cuantitativos relacionados con la historia natural de la enfermedad cuando se usa sólo orquidectomía para el manejo.
Tipos de tumores germinales de testículoPara efectos prácticos, los tumores germinales de testículo se dividen en dos grupos: seminomas y no seminomas. Esta distinción es crítica para la toma de decisiones terapéutica, seguimiento y pronóstico. El patólogo nos indica si es un seminoma o no. En caso de que haya componente no seminomatoso en el espécimen tumoral, se debe considerar como no seminoma para todos los efectos de manejo. Una minoría de seminomas exhiben elevación de beta-hCG, pero la elevación de alfa fetoproteina (AFP) es característica de no seminomas y su elevación significa que no se trata de un seminoma. Aproximadamente la mitad de los tumores germinales de testículo son seminomas. Los seminomas tienden a ser más radiosensibles que los no seminoas.
Estudios de extensión de la enfermedadLos pacientes con tumores germinales de testículo deben ser estudiados con TAC de tórax, abdomen y pelvis contrastado, LDH, beta-hCG y AFP para establecer la extensión de la enfermedad.
Sistema TNMS y EstadioPara poder diseñar el tratamiento más apropiado de los pacientes con tumores germinales de testículo se deben estatificar apropiadamente y para eso utilizamos el TNMS, así (1)
Definiciones TNM Tumor Primario (T)pTX: No puede evaluarse el tumor primario*
pT0: No hay constancia de tumor primario (por ejemplo, cicatriz histológica en el testículo)
pTis: Neoplasia celular Intratubular (carcinoma in situ)
pT1: Tumor limitado al testículo y epidídimo sin invasión linfático/vascular;
el tumor podría invadir la túnica albuginea pero no la túnica vaginalis
pT2: Tumor limitado al testículo y epidídimo con invasión linfático/vascular o tumor extendiéndose a través de la túnica albugínea involucrando la túnica vaginalis
pT3: Tumor invade el cordón espermático con invasión linfático/vascular o sin esta
pT4: Tumor invade el escroto con invasión linfático/vascular o sin esta
*[Nota: La extensión del tumor primario se clasifica por medio de la orquiectomía radical excepto para pTis y pT4. El TX se podría emplear para otras categorías en la ausencia de una orquiectomía radical.]
Ganglios linfáticos regionales (N)NX: No pueden evaluarse los ganglios linfáticos regionales
N0: No hay metástasis regional de ganglios linfáticos
N1: Metástasis con un solo ganglio linfático, ≤2 cm en su dimensión mayor; o ganglios linfáticos múltiples de ≤2 en su mayor dimensión.
N2: Metástasis en un solo ganglio linfático, protuberancia >2 cm pero ≤5 cm en su dimensión mayor; o ganglios linfáticos múltiples, ≤5 cm en su dimensión mayor
N3: Metástasis con una protuberancia de un ganglio linfático >5 cm en la dimensión mayor.
Metástasis a distancia (M)MX: No puede evaluarse la presencia de metástasis a distancia
M0: No hay metástasis a distancia
M1: Metástasis a distancia
M1a: Metástasis pulmonar nodal o no regional
M1b: Metástasis distante además de los ganglios linfáticos no regionales y los pulmones
Marcadores tumorales séricos (S)SX: Estudios sobre marcadores no realizados o disponibles
S0: Los grados de estudio de los marcadores, dentro de los límites de normalidad
S1: Lactatodeshidrogenasa (LDH) <1,5 X N* y Gonadotropina coriónica humana (hCG) (mIU/mL) <5000 y Alfa fetoproteína (AFP) (ng/mL) <1,000
S2: LDH 1,5-10 X N* o hCG (mIU/mL) 5000-50,000 o AFP (ng/mL) 1,000-10,000
S3: LDH > 10 X N* o hCG (mIU/mL) >50,000 o AFP (ng/mL) >10,000
* [Nota: N indica el límite óptimo de lo normal para la prueba del LDH.]
Agrupación por estadíosEstadio 0: pTis, N0, M0, S0
Estadio I: pT1-4, N0, M0, SX
Estadio IA: pT1, N0, M0, S0
Estadio IB: pT2, N0, M0, S0; pT3, N0, M0, S0; pT4, N0, M0, S0
Estadio IS: Cualquiera pT/Tx, N0, M0, S1-3
Estadio II: Cualquiera pT/Tx, N1-3, M0, SX
Estadio IIA: Cualquiera pT/Tx, N1, M0, S0; Cualquiera pT/Tx, N1, M0, S1
Estadio IIB: Cualquiera pT/Tx, N2, M0, S0; Cualquiera pT/Tx, N2, M0, S1
Estadio IIC: Cualquiera pT/Tx, N3, M0, S0; Cualquiera pT/Tx, N3, M0, S1
Estadio III: Cualquiera pT/Tx, cualquiera N, M1, SX
Estadio IIIA: Cualquiera pT/Tx, cualquiera N, M1a, S0-1
Estadio IIIB: Cualquiera pT/Tx, N1-3, M0, S2; Cualquiera pT/Tx, cualquiera N, M1a, S2
Estadio IIIC: Cualquiera pT/Tx, N1-3, M0, S3; Cualquiera pT/Tx, cualquiera N, M1a, S3; Cualquiera pT/Tx, cualquiera N, M1b, cualquiera S.
Agrupación pronóstica en enfermedad metastásicaEn vista de que los resultados con quimioterapia para tumores germinales metastáticos es altamente eficaz, se ha buscado la manera de identificar subgrupos de mejor pronóstico para poder diseñar la terapia óptima con la menor toxicidad posible. Se recomienda utilizar la IGCCC de 1977 asi (2):
SEMINOMAPronóstico favorable Cualquier lugar primario y sin metástasis no pulmonares viscerales y AFP normal, cualquier hCG, cualquier LDH
Pronóstico intermedioCualquier lugar primario, y con metástasis no pulmonares viscerales, y un AFP normal, cualquier hCG, cualquier LDH
NO SEMINOMAPronóstico favorableTestículo/primario retro peritoneal, y sin metástasis no pulmonares viscerales, y buenos marcadores - de todos: Alfa fetoproteína (AFP) <1,000 ng/mL y gonadotropina coriónica humana (hCG) <5,000 IU/L (1,000 ng/mL) y Lactato deshidrogenasa (LDH) <1,5 X el límite superior de lo normal
Pronóstico intermedio Testículo/primario retro peritoneal, y sin metástasis no pulmonares viscerales, y marcadores intermediarios - cualquiera de: AFP 1,000 - 10,000ug/mL o hCG ≥5,000 - 50,000 IU/L o LDH ≥1,5 X N* y ≥10 X N*
Pronóstico maloPrimario mediastínico o metástasis no pulmonares viscerales o marcadores precarios - cualquiera de: AFP >10,000 ng/mL o hCG >50,000 IU/mL (10,000 ng/mL) o LDH >10 X el limite superior de lo normal
Historia natural (3)SEMINOMALos pacientes con seminoma estadío I tratados con orquidectomía tienen un riesgo de recurrencia de aproximadamente el 20%. La inmensa mayoría ocurren en el retroperitoneo abdominal. El tiempo de recurrencia mediano es de 12-18 meses, con 30% de las recurrencias después de 2 años y 5% de ellas después de 5 años. Los seminomas son muy radiosensibles y la radioterapia post-orquidectomía es una modalidad muy utilizada en otras partes del mundo para el manejo de seminomas estadíos I y II. La recurrencia post-radioterapia es del 4%, 6% y 51% en pacientes con estadíos I, IIA/B y IIC, respectivamente. Aproximadamente el 90% de los seminomas metastáticos pertenecen al grupo de bajo riesgo con supervivencia libre de progresión a los 5 años de 82% y supervivencia a 5 años de 86%. El 10% restante de los seminomas metastáticos pertenecen al grupo de riesgo intermedio con supervivencia libre de progresión a los 5 años de 67% y supervivencia a 5 años de 72%.
NO SEMINOMAS Los no seminomas estadío I tratados con orquidectomía tienen un riesgo de recurrencia del 15% si son estadío IA y 50% si son estadío IB. El tiempo mediano para la recurrencia es de aproximadamente 12 meses. Es rara la recaida después de 2 años, y las recaidas después de 5 años son exóticas. A diferencia de los seminomas, los no seminomas han sido caracterizados como relativamente radioresistentes y la estrategia de manejo para estadíos I, IIA/B incluyen cirugía: la disección ganglionar retroperitoneal o RPLND por sus siglas en inglés que consiste en la disección de los ganglios paraaórticos, preaórticos, retroaórticos, interaortocavas, paracavas, retrocava y precavas desde los hilios renales hasta los ganglios de las cadenas ilíacas comunes bilaterales. La mortalidad de RPLND es de aproximadamente 1%. La complicación a largo plazo más temida es la eyaculación retrógrada que ocurre en 50% con las técnicas antiguas y se disminuyen al 5% en pacientes bajo el cargo de cirujanos con amplia experiencia en el procedimiento que utilizan las nuevas técnicas de preservación de nervio. La recurrencia retroperitoneal después del RPLND es esencialmente nula y no se requiere de imágenes de seguimiento rutinarias de este sitio en el seguimiento postoperatorio. Aproximadamente el 56% de los no seminomas metastáticos pertenecen al grupo de bajo riesgo con supervivencia libre de progresión a los 5 años de 89% y supervivencia a 5 años de 92%. El 26% de los no seminomas metastáticos pertenecen al grupo de riesgo intermedio con supervivencia libre de progresión a los 5 años de 75% y supervivencia a 5 años de 80%. El 16% restante de los no seminomas metastáticos pertenecen al grupo de riesgo alto con supervivencia libre de progresión a los 5 años de 41% y supervivencia a 5 años de 48%.
Recomendaciones de manejo inicial en pacientes con tumores germinales de testículoA continuación se estipulan las recomendaciones de manejo inicial post orquidectomía de pacientes con tumores germinales de testículo.
SEMINOMAEstadío I
En seminoma estadío I, a diferencia de en los no seminomas, la presencia de marcadores tumorales elevados no cambia el manejo (con la notable excepción de la AFP pues su elevación indica que se trata de un no seminoma). Por lo tanto, las recomendaciones de manejo para estadíos IA, IB y IS son esencialmente iguales. El estándar de tratamiento en los Estados Unidos es radioterapia con dosis de 2000-3000 cGy en fracciones de 180 cGy por día a los ganglios paraaórticos con inclusión de los ganglios ilíacos en situaciones especiales (T4). No se recomienda radioterapia en pacientes con riñón en herradura o pélvico, enfermedad inflamatoria intestinal o historia de radioterapia previa. Una vez terminada la radioterapia, se recomienda seguimiento así (4): Historia clínica y examen físico, LDH, AFP, Beta hCG cada 3-4 meses por 1 año, cada 6 meses en el año 2, luego cada año; TAC abdómino / pélvico cada año x3; Rayos X de tórax cada otra visita. La probabilidad de recurrencia luego de radioterapia es de aproximadamente 4%.
La otra opción de manejo es el seguimiento estricto o surveillance. Esta estrategia debe ser practicada en pacientes altamente motivados que estén dispuestos a cumplir con un esquema consistente en: Historia clínica y examen físico, LDH, AFP, Beta hCG cada 3-4 meses por 3 años, cada 6 meses del año 4 al 7, luego cada año; TAC abdomino / pélvico con cada visita; Rayos X de tórax cada otra visita. Se recomienda seguimiento hasta los 10 años.
Otra forma de tratar estos pacientes es con quimioterapia con un ciclo de carboplatino AUC de 7. En un estudio de 1477 pacientes aleatorizados entre radioterapia o carboplatino se encontró una supervivencia libre de progresión a 3 años de 95.9% comparado con 94.8%. Los pacientes tratados con carboplatino tuvieron menos incapacidad, menos letargia y menor frecuencia de segundos primarios testiculares que los tratados con radioterapia (5). Se ha criticado que los resultados fueron publicados con un seguimiento relativamente corto para seminoma.
La recomendación de manejo post orquidectomía en pacientes con seminoma estadío I debe ser individualizada, sin embargo, el manejo con un ciclo de quimioterapia con carboplatino parece una alternativa eficaz y segura para este grupo de pacientes.
Estadío II
Todos los pacientes con seminoma estadío II requieren de terapia post orquidectomía o su mortalidad es del 100%. Las opciones de tratamiento incluyen radioterapia radioterapia con dosis de 3500-4000 cGy en fracciones de 180 cGy por día a los ganglios paraaórticos con inclusión de los ganglios ilíacos. En pacientes con contraindicaciónes para radioterapia o con enfermedad muy voluminosa se puede utilizar quimioterapia basada en cisplatino (el carboplatino es claramente inferior al cisplatino en enfermedad mayor que el estadío I, y no se recomienda su uso en forma rutinaria). La radioterapia es claramente insuficiente en pacientes con estadío IIC por la alta probabilidad de recaida en este grupo de pacientes luego de esta modalidad.
Estadío III
El seminoma metastático se trata con quimioterapia basada en cisplatino.
Esquema y duración de quimioterapia en seminoma estadíos II y III
Considerable controversia ha surgido con la elección del esquema que ha de utilizarse en pacientes con tumores germinales de testículo. Está claro que el cisplatino es fundamental y la dosis es de 100 mg/m2 por ciclo cada 3 semanas. También sabemos que el etopósido es superior a la vinblastina por menor toxicidad neuromuscular y mejor eficacia en enfermedad avanzada (6). La dosis de etopósido debe ser 500 mg/m2 por ciclo pues esta es superior a los 360 mg/m2 que se utilizaba en Europa en el pasado (3). El esquema puede ser administrado en 3 o 5 días, siempre y cuando se administre la dosis total (7).
Cuatro ciclos de etopósido + cisplatino o EP como es conocido son eficaces en pacientes con estadío II y en pacientes estadío III de bajo riesgo. Otra alternativa es el uso de BEP x3 ciclos, en la que se adiciona bleomicina al EP convencional a los pacientes con seminoma estadío III de bajo riesgo. En pacientes con seminoma estadío III de riesgo intemedio se recomienda BEP x4 ciclos (en este grupo se considera insuficiente el tratamiento con 2 medicamentos y se recomienda la adición de la bleomicina). La bleomicina tiene toxicidad pulmonar importante, especialmente si se pasa de 300 U (10 semanas de tratamiento). Se considera que la toxicidad por bleomicina es trivial cuando se usan 3 ciclos de BEP con una mortalidad por toxicidad pulmonar por bleomicina menor del 1% (8).
Toxicidades con el tratamiento
La radioterapia causa astenia, toxicidad gastrointestinal, limita la dosis de quimioterapia que se puede utilizar en el futuro si hay recaída e incrementa la probabilidad de muerte por neoplasias malignas secundarias y por enfermedad cardiovascular (9). El incremento en la mortalidad cardiovascular y por neoplasias secundarias se observa después de 15 años y no es trivial (38 exceso de muertes en una cohorte de 453 pacientes). Claro está que sin tratamiento post orquidectomía, aproximadamente 160 pacientes de esos 453 habrían fallecido por seminoma.
La quimioterapia también causa incremento en la mortalidad cardiovascular y en el riesgo de neoplasias secundarias. Otras toxicidades asociadas a la quimioterapia incluyen: náuseas, vómito, alopecia reversible, daño transitorio o permanente al riñón, neuropatía periférica, ototoxicidad, hipokalemia, hipomagnesemia, mielosupresión con riesgo de neutropenia febril de 7-15%, fenómeno de Raynaud y toxicidad pulmonar. El fenómeno de Raynaud ocurre en el 8% de los pacientes que reciben terapia con bleomicina y la toxicidad pulmonar también ocurre por la bleomicina y constituye la causa de la mitad de las muertes post tratamiento en pacientes con tumores germinales de testículo. Los riesgos de toxicidad por bleomicina son mayores en personas mayores, en pacientes con enfermedad pulmonar preexistente y en pacientes con disfunción renal.
En la práctica del autor se favorece el uso de BEP por cierta tendencia a los estudios a demostrar que hay un mejor control antineoplásico con la adición de la Bleomicina. En situaciones de bajo riesgo se utiliza BEP x3 y en riesgo intermedio se utiliza BEP x4. Para pacientes mayores de 50 años, fumadores, con enfermedad pulmonar preexistente o con creatinina mayor de 2 mg/dL, se utiliza EP (8).
Seguimiento post quimioterapia
El seguimiento post quimioterapia en seminoma es idéntico al no seminoma. Se recomienda: Evaluación clínica, beta hCG, AFP, LDH, rayos X de tórax cada 2-3 meses en años 1-2; cada 4 meses en años 3-4; cada 6 meses en año 5; cada 12 meses en año 6+. Se recomienda TAC abdómino pélvico cada 6 meses año 1
Cada 6-12 meses año 2; cada 12 meses año 3-5; cada 12-24 meses año 6+ (4)
NO SEMINOMAComo ya mencionamos, el tratamiento del no seminoma temprano es distinto al del seminoma. El no seminoma es considerado menos radiosensible y la cirugía juega un papel más importante en el manejo.
Estadío IA
Las opciones de tratamiento para no seminoma estadío IA es RPLND o surveillance. El surveillance se hace así: Evaluación clínica, LDH, beta hCG, AFP y rayos X de tórax cada 1-2 meses en año 1; cada 2 meses en año 2; cada 3 meses en año 3; cada 4 meses en año 4; cada 6 meses en año 5; cada año, luego de 6 años. Además se recomienda TAC abdómino pélvico cada 2-3 meses en año 1; cada 3-4 meses en año 2; cada 4 meses en año 3; cada 6 meses en año 4; cada año en años 5+. En caso de que se elija surveillance, se recomienda una adherencia estricta. El riesgo de recurrencia es del 15% y 2/3 de estas ocurren en el retroperitoneo. La quimioterapia no está indicada en este estadío.
Estadío IB
La probabilidad de recaida es de aproximadamente el 50% en pacientes con no seminomas estadío IB. El surveillance sólo se recomienda en pacientes muy seleccionados altamente motivados. Otras opciones de tratamiento son la RPLND o 2 ciclos de quimioterapia con BEP.
Si durante la RPLND se encuentra enfermedad neoplásica N1 o N2, se debe practicar 2 ciclos de quimioterapia con BEP o EP. En caso de encontrarse enfermedad N3 (tumores de más de 5 cm), se recomienda consolidar con 4 ciclos de EP o 3 ciclos de BEP.
El seguimiento post PRLND es idéntico al seguimiento post quimioterapia, excepto por la no necesidad de imágenes abdominales por el bajo riesgo de recurrencia en este grupo de pacientes a ese nivel luego de la cirugía (ver arriba).
Estadío IS
En los no seminomas, la persistencia de marcadores tumorales elevados indica persistencia de enfermdad. En esto difieren de los seminomas. La recomendación de manejo para pacientes con estadío I con persistencia de marcadores elevados es quimioterapia con EP x4 o BEP x3. Hay que tener en cuenta cuenta que la beta hCG tiene una vida media de 18-36 horas y la de la AFP es de 5-7 días, pues si los valores son elevados al momento de la orquidectomía, su disminución puede tomar varias semanas sin ser indicativo de enfermedad persistente (especialmente para la AFP).
Estadío IIA o IIB Con marcadores elevados (S1)
Se tratan igual que el estadío IS con EP x4 o BEP x3.
Estadíos IIA o IIB Sin marcadores elevados (S0)
Estos pacientes pueden tratarse con RPLND o con quimioterapia con BEP x3. En general se favorece la quimioterapia si la enfermedad es multifocal o metástasis fuera del drenaje linfático esperado. En los Estados Unidos la RPLND es el estándar más utilizado. Entre nosotros se utiliza más la quimioterapia.
Estadíos IIC y III
Los pacientes con estadío IIC y III se tratan con quimioterapia. Para pacientes con estadío IIC se considera suficiente BEP x3 o EP x4. En pacientes con estadíos IIIA y IIIB y IIIC se recomienda BEP x4 como terapia estándar. Los pacientes con estadío IIIC de alto riesgo tienen una probabilidad de curación comparativamente baja de menos del 50% y serían candidatos a estudios clínicos, incluyendo aquellos que utilizan terapia de altas dosis con rescate con células madres hematopoyéticas (autotrasplante de médula ósea).
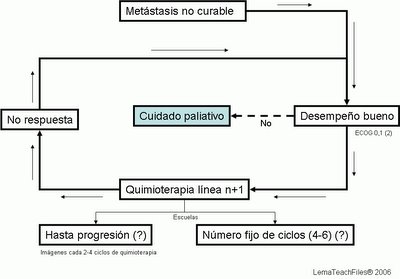
Una vez terminado el curso de quimioterapia propuesto, se debe valorar la respuesta. Si hay respuesta completa, se recomienda observación. Si hay respuesta parcial, se recomienda resección de la lesión(es) residual(es). Si no hay respuesta, se recomienda quimioterapia de segunda línea con ifosfamida. El pronóstico es particularmente pobre en este último grupo de pacientes.
Referencias1. Testes. In: American Joint Committee on Cancer.: AJCC Cancer Staging Manual. 6th ed. New York, NY: Springer, 2002, pp 317-322
2. International Germ Cell Consensus Classification: a prognostic factor-based staging system for metastatic germ cell cancers. International Germ Cell Cancer Collaborative Group. J Clin Oncol 15 (2): 594-603, 1997
3. DeVita VJ, Hellman S, Rosenberg SA (eds): Chapter 31, in Cancer: Principles and Practice (ed 7). Philadelphia, PA, Lippincott Williams & Wilkins, 2005, pp 1269–1293
4. National Comprehensive Cancer Network (NCCN): http://www.nccn.org/ accesado en 05/11/2006
5. Oliver RT, Mason M, Mead GM, et al; MRC TE19 collaborators and EORTC 30982 collaborators. Radiotherapy versus single-dose carboplatin in adjuvant treatment of stage I seminoma: a randomized trial. Lancet. 2005;366(9482):293-300 PMID: 16039331
6. Williams, SD, Birch, R, Einhorn, LH, et al. Treatment of disseminated germ-cell tumors with cisplatin, bleomycin, and either vinblastine or etoposide. N Engl J Med 1987 316: 1435-1440. PMID: 2437455
7. de Wit R, Roberts JT, Wilkinson. PM et al. Equivalence of Three or Four Cycles of Bleomycin, Etoposide, and Cisplatin Chemotherapy and of a 3- or 5-Day Schedule in Good-Prognosis Germ Cell Cancer: A Randomized Study of the European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group and the Medical Research Council J Clin Oncol 2001 19: 1629-1640 PMID: 11250991
8. Einhorn LH, Foster RS. Bleomycin, Etoposide, and Cisplatin for Three Cycles Compared With Etoposide and Cisplatin for Four Cycles in Good-Risk Germ Cell Tumors: Is There a Preferred Regimen? J Clin Oncol 2006 24: 2597-2598 PMID: 16735718
9. Zagars GK, Ballo MT, Lee AK, Strom SS. Mortality after cure of testicular seminoma. J Clin Oncol 2004; 22: 640-647. PMID: 14726503